Shimadzu HPLC Blog: Selektivita (α)
- Foto: Gesa Schad (Product Manager at Shimadzu Europa GmbH): My LC Blog: Selektivita (α)
- Video: Shimadzu Scientific Instruments: LC Theory and Key Principles: Session 3
V minulých dílech Shimadzu HPLC Blogu jsme probrali tato témata:
- Díl 01: Začínáme
- Díl 02: Základní teorie
- Díl 03: Separační módy
- Díl 04: Chromatografie na reverzních fázích
- Díl 05: Izokratická vs. Gradientová eluce
- Díl 06: Anatomie HPLC instrumentace
- Díl 07: Detektory
- Díl 08: LCMS detektor
- Díl 09: Rovnice rozlišení
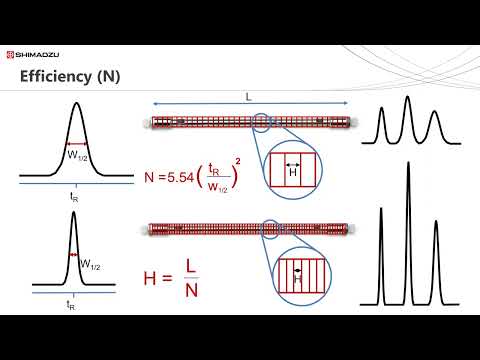
- Díl 10: Účinnost kolony
- Díl 11: Retenční faktor (k)
Jedním z nejužitečnějších pojmů v praktickém vývoji HPLC/UV metody je separace kritických párů pomocí ladění selektivity. Dnes se podíváme na to, co znamená „selektivita“ a jaké parametry ji ovlivňují, abychom je mohly využít ke zlepšení LC separace.
Selektivita (α) je definována jako rozdíl v relativní retenci dvou analytů pro dané podmínky stacionární fáze a mobilní fáze. Jinými slovy, α je měřítkem vzdálenosti mezi píky. Popisuje separaci dvou píků vzájemně vůči sobě a lze ji vypočítat jako poměr mezi retenčními faktory k2 a k1 dříve a později eluovaných píků (obrázek 1).
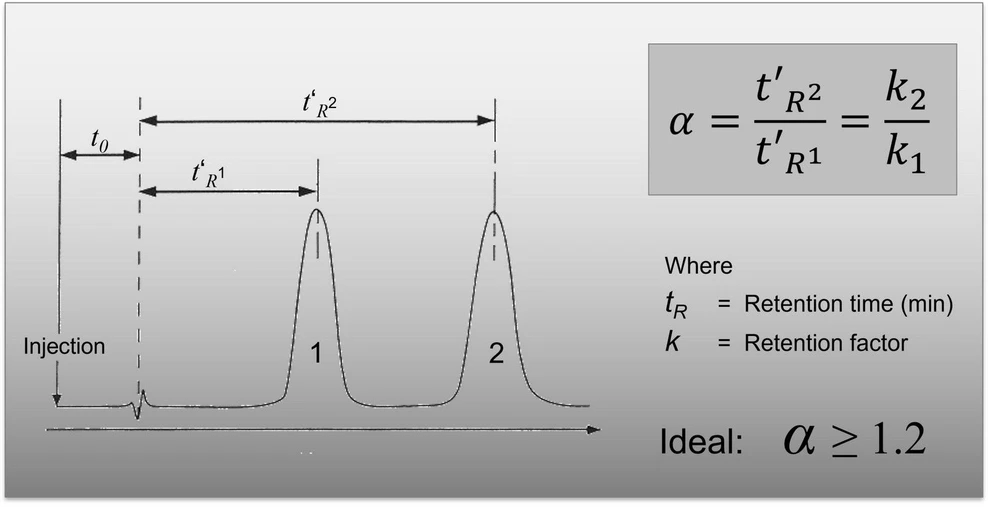 Shimadzu HPLC Blog: Obrázek 1 Rovnice a vizuální znázornění výpočtu selektivity pro dva analyty
Shimadzu HPLC Blog: Obrázek 1 Rovnice a vizuální znázornění výpočtu selektivity pro dva analyty
Podrobnosti o retenci a výpočtu k naleznete v článku Shimadzu HPLC Blog: Retenční faktor (k). Retenční faktor (k) a selektivita (α) jsou ovlivněny parametry, které určují retenci. Selektivitu lze tedy změnit změnou chemického složení stacionární fáze a složení mobilní fáze. Jaký je tedy rozdíl, ptáte se? K pochopení Vám pomůže obrázek z předchozího článku.
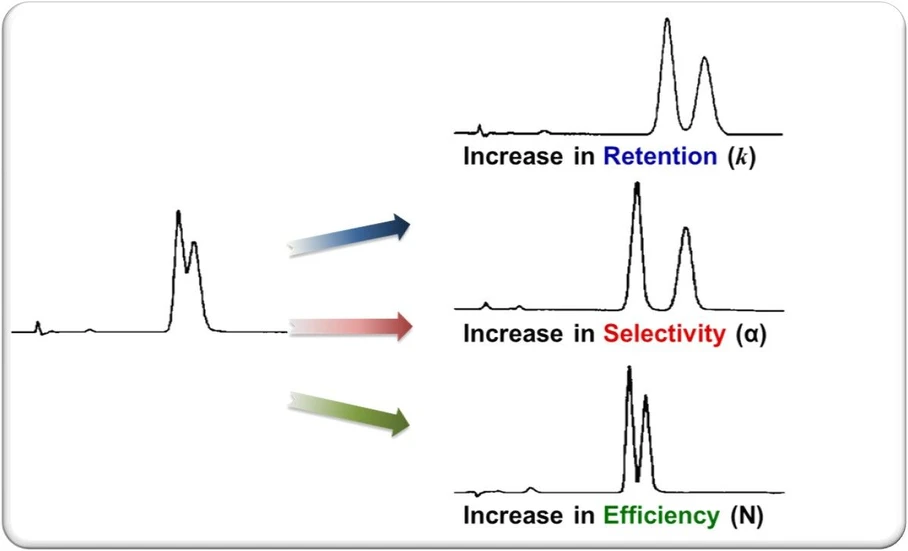 Shimadzu HPLC Blog: Obrázek 2 - Vizuální příklad vlivu retence, selektivity a účinnosti na rozlišení
Shimadzu HPLC Blog: Obrázek 2 - Vizuální příklad vlivu retence, selektivity a účinnosti na rozlišení
Na obrázku 2 vidíte, jak zvýšení retence může vést k lepšímu rozlišení, ale vždy za cenu delší retenční doby, což v izokratické analýze také vede k širším píkům. Při zvýšení selektivity nemusíte nutně zvyšovat retenci, ale spíše ji změnit tak, aby ovlivňovala různé sloučeniny v různé míře, a tím zvětšila prostor mezi nimi. To může znamenat snížení retence pro jednu sloučeninu, ale její zachování pro druhou eluující sloučeninu.
Při vývoji metody by to pravděpodobně znamenalo, že v screeningovém experimentu identifikujete vhodnou kombinaci stacionární a mobilní fáze, abyste dosáhli adekvátní retence a určité separace. Odtud přejdete k optimalizaci metody tím, že se podíváte na další parametry, které ovlivňují selektivitu, abyste zlepšili separaci. V posledním článku jsme se zabývali vlivem změn % organického modifikátoru na retenci, takže to je jedna možnost, kterou můžete zvážit, a také změny pH vodné mobilní fáze a teploty kolony budou s největší pravděpodobností mít za následek posun píků. Ukážeme si to na několika příkladech.
Začněme teplotou. Podle Van 't Hoffovy rovnice, pokud bychom vynesli log k vs. 1/T (v Kelvinech), dostali bychom přímku, která ilustruje, že vyšší teplota obecně snižuje retenci a vede k ostřejším píků analytů, protože ovlivňuje viskozitu mobilní fáze. Teplota však ovlivňuje také rozpustnost a ionizaci analytu, stejně jako ionizaci nabitých funkčních skupin stacionární fáze, což vede ke změnám retenčního chování různých analytů, jak je vidět na příkladu na obrázku 3.
 Shimadzu HPLC Blog: Obrázek 3 - Příklad separace ukazující vliv teploty na selektivitu
Shimadzu HPLC Blog: Obrázek 3 - Příklad separace ukazující vliv teploty na selektivitu
Zatímco pokles teploty o 5 °C a poté o 11 °C vede u většiny analytů k mírnému zvýšení retence, u sloučeniny 6 je tento účinek mnohem výraznější a zvyšuje rozlišení kritického páru (5, 6) až k separaci na základní linii.
Vliv změn pH může být mnohem méně výrazný, pokud se ionizace nabitých skupin změní v důsledku podmínek mobilní fáze. Ukážeme si to na příkladu vitamínů rozpustných ve vodě a zejména na pohyb kyseliny listové a kyseliny p -aminobenzoové. Strukturní vzorce a ionizovatelné funkční skupiny pro obě sloučeniny jsou uvedeny na obrázku 4.
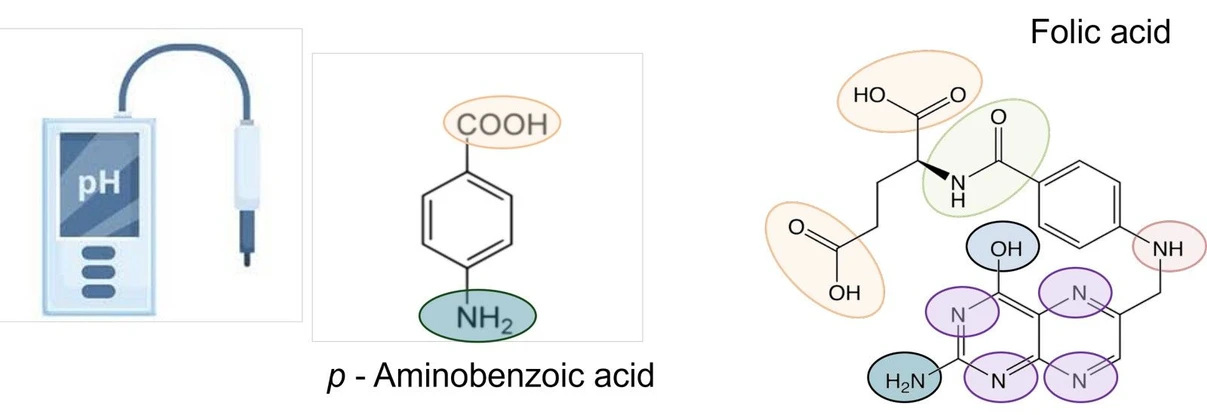 Shimadzu HPLC Blog: Obrázek 4 - Strukturní vzorec kyseliny p -aminobenzoové a kyseliny listové s vyznačenými ionizovatelnými funkčními skupinami
Shimadzu HPLC Blog: Obrázek 4 - Strukturní vzorec kyseliny p -aminobenzoové a kyseliny listové s vyznačenými ionizovatelnými funkčními skupinami
Při pH ekvivalentním pKa kyselé nebo zásadité analyzované látky bude 50 % molekul nabitých, zatímco 50 % zůstane neutrálních, což může vést k rozštěpení nebo rozšíření píku pro danou sloučeninu. Při zvažování pH mobilní fáze je proto nejlepší držet se daleko od pKa (+/- 1,5), aby byla analyzovaná látka buď plně nabitá, nebo nenabitá. Při práci s řadou analytů, z nichž některé nesou více ionizovatelných skupin, to však nemusí být vždy možné. Obrázek 5 ukazuje separaci vitamínů rozpustných ve vodě, včetně p-aminobenzoové kyseliny a kyseliny listové, kde byla vodná mobilní fáze upravena na pH 2,2, 2,7 a 3,5.
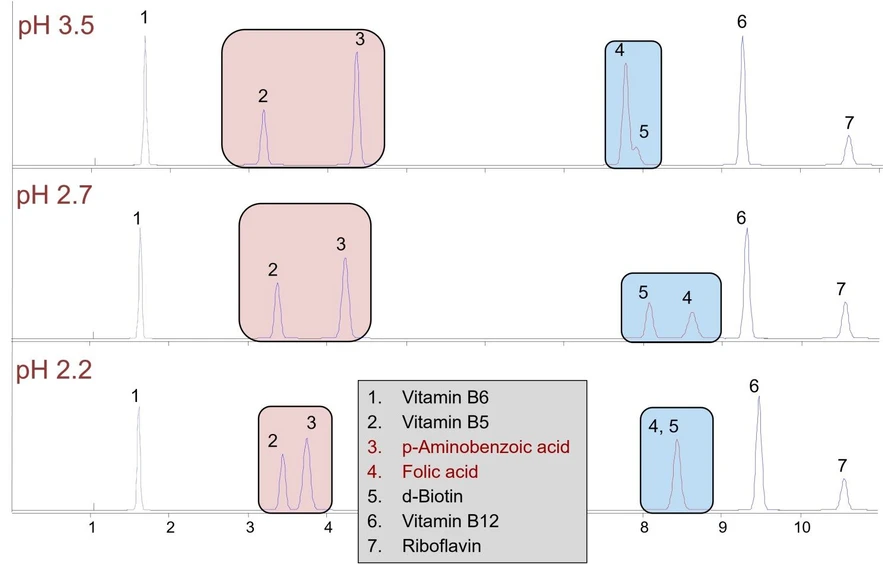 Shimadzu HPLC Blog: Obrázek 5 - HPLC separace vitamínů rozpustných ve vodě s různým pH mobilní fáze
Shimadzu HPLC Blog: Obrázek 5 - HPLC separace vitamínů rozpustných ve vodě s různým pH mobilní fáze
Při pohledu na kyselinu p-aminobenzoovou vidíme, že pík (3) se s klesajícím pH posouvá ke kratší retenci, protože karboxylová kyselina (pKa = 2,7) se mění z nenabité na nabitou, což znamená, že je polárnější. Pík 4 s více ionizovatelnými skupinami se naopak chová méně předvídatelně a vykazuje silný nárůst retence s poklesem pH z 3,5 na 2,7. Při dalším poklesu pH na 2,2 se však posune ke kratší retenci a koeluuje s píkem 5. Podrobnější vysvětlení role pH na retenci a selektivitě najdete v článku Johna Dolana publikovaném v LCGC: Zpátky k základům: Role pH v retenci a selektivitě.
Dalšími faktory, které byste měli při změně selektivity uvažovat, jsou výběr mobilní fáze s ohledem na iontovou sílu, pH nebo výběr pufru. O tom si povíme v dalším díle Shimadzu HPLC Blogu. Pokud se chcete předtím o tématu vývoje metod dozvědět více, doporučuji Snyder, L. R., Kirkland, J. J. & Glajch, J. L. (2012); Practical HPLC Method Development, John Wiley & Sons, Inc.
Edukativní HPLC a LC/MS webinaře Shimadzu
- Introducing Shimadzu's Analytical Intelligence in AQbD Method Development
- Chromatography Unleashed: Elevate Your Chiral and Achiral Separations
- Shimadzu's LC Method Development (RP) Series - Session 1: Method Screening
- MALDI-Imaging For All: A Researcher’s Guide
- Analytical Technologies for COVID-19 Challenges: Drug Repurposing | Vaccine Research | PPE & Material Testing | Environmental Monitoring
Výběr literatury Shimadzu se zaměřením na základy a principy HPLC a LC/MS v knihovně LabRulezLCMS
- Back to Basics - Explaining Resolution (Technické články | 2020)
- Back to Basics - Gradient Retention Factor, K* (Technické články | 2020)
- Back to Basics - Dispersion - Protocols for LC Instruments (Technické články | 2020)
- RF-20A Fluorescence Detector Basics and Applications (Technické články | 2010)
- Back to Basics - Gradient Anatomy - Protocols for LC Instruments (Technické články | 2020)
- The Very Basics of IMAGEREVEAL MS - With differential analysis as an example (Prezentace)
- Back to Basics - Pump Linearity and Dwell Volume Measurements - Protocols for LC Instruments (Technické články | 2020)
- Improving the Yield of Basic Amino Acids in a Protein Sequencer (Aplikace | 2023)
- SFC Basic Guide - Shimadzu Supercritical Fluid Chromatograph (Příručky | 2021)
- Rewriting the Book on Supercritical Fluid Chromatography (Technické články | 2024)




