Přehled analytických metod pro stanovení fytové kyseliny

Pixabay/Pexels: Přehled analytických metod pro stanovení fytové kyseliny
Fytová kyselina je hlavní zásobní forma fosforu v obilných zrnech. Vyskytuje se ve formě smíšených solí (fytátů). Tato forma fosforu je obtížně stravitelná pro monogastrická zvířata i pro člověka. Během průchodu trávicím traktem může fytát vázat některé esenciální stopové prvky a minerály a negativně tak ovlivňuje využitelnost živin a dalších nutričně cenných látek, na druhé straně vykazuje řadu pozitivních zdravotních účinků. Je silným antioxidantem, snižuje riziko řady civilizačních chorob, inhibuje krystalizaci vápníku a brání tvorbě ledvinových kamenů. Má také pozitivní vliv na hladinu glukosy v krvi a cholesterolu. Proto jsou role fytátu v lidské výživě a jeho vliv na zdraví nadále intenzivně studovány. Tato práce shrnuje vývoj analytických postupů pro stanovení fytové kyseliny v obilovinách i dalších matricích od nejstarší metody srážení nerozpustného fytátu železitého v kyselém roztoku, přes kolorimetrické metody až po mnoho druhů moderních instrumentálních metod, jakými jsou například nukleární magnetická rezonance, izotachoforéza a vysokoúčinná kapalinová chromatografie.
1 ÚVOD
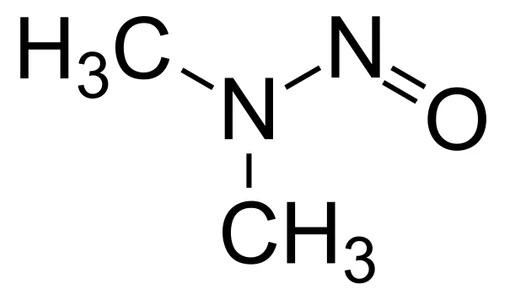
Fytová kyselina byla objevena v letech 1855 až 1856, kdy Hartig poprvé identifikoval malé kulaté částice veliké jako zrna bramborového škrobu, nalezené v semenech různých rostlin (Hartig, 1855; 1856). Použití jodového testu ukázalo, že tyto částice škrob neobsahují, což vedlo k závěru, že musí obsahovat rezervní výživné látky pro klíčení semen. Později bylo zjištěno, že izolované částice jsou bohaté na fosfor, vápník a hořčík, ale neobsahují bílkoviny ani tuky (Pfeffer, 1872). Název fytin (phytin) byl vytvořen na základě skutečnosti, že tato látka je rostlinného původu, nebyla nalezena v mase ani v mléčných výrobcích a byla původně charakterizována jako ložiska vápenato-hořečnatého fytátu v semenech rostlin. Bylo zjištěno, že hydrolýzou fytinu pomocí HCl se uvolní kyselina fosforečná a inositol. O možné struktuře fytové kyseliny se diskutovalo mnoho let a v roce 1914 Anderson (Anderson, 1914) představil molekulární strukturu myoinositol-1,2,3,4,5,6-hexakisdihydrogenfosfátu (IP6), také zvaného fytová kyselina (obr. 1), která byla potvrzena moderními analytickými metodami a platí dodnes. Je to jednoduchý cyklický sacharid se šesti fosfátovými skupinami navázanými na každém atomu uhlíku. Při pH 0,5–9,0 vytváří stericky stabilní strukturu, kdy je konformace fosforečných skupin v uspořádání 5 axiálně a 1 ekvatoriálně (Emsey, Niazi, 1981).
 Obr. 1 Struktura fytové kyseliny
Obr. 1 Struktura fytové kyseliny
Při fyziologickém pH (6,0–7,0) jsou silné negativní náboje molekuly vyváženy pravděpodobně sodnými nebo jinými ionty. Tato jedinečná struktura s 12 vyměnitelnými protony a vysokou hustotou záporně nabitých fosfátových skupin je zodpovědná za charakteristické vlastnosti umožňující tvorbu velmi stabilních komplexů s polyvalentními kationty.
2 VÝSKYT FYTOVÉ KYSELINY
Fytát, sůl fytové kyseliny, je hlavní formou zásobního fosforu v semenech rostlin: představuje 50–85 % fosforu v jádrech obilovin, olejnin a luštěnin (Irvine, 2005). Kromě fytátu jsou v semenech v mnohem menším množství (do 15 %) přítomny i nižší inositolfosfáty, jako inositolpentakisfosfáty a inositoltetrakisfosfáty. Při klíčení semen je fytát enzymaticky hydrolyzován a uvolňuje se fosfát, který je rostlinou spolu s minerály vápníkem a hořčíkem zužitkován při klíčení. Fytát převládá v nezpracovaných potravinách, během zpracování je degradován na nižší inositolfosfáty.
Hlavními zdroji fytátu v každodenní stravě jsou obilniny, luštěniny, olejniny a ořechy. Představují 40 až 60 % celkového dietárního příjmu člověka. V obilninách se fytát nachází v aleuronové vrstvě (přibližně 80 %) a klíčku, zatímco v endospermu se téměř nevyskytuje. Obilniny obsahují průměrně 1 % fytové kyseliny v sušině, v rozmezí od 0,06 do 2,2 % (tab. 1). Některé obilné produkty však mají vyšší obsah fytové kyseliny (Wise, 1983), např. v pšeničných klíčcích a pšeničných otrubách se její hladiny pohybovaly od 1,1 do 7,3 %, v rýžových otrubách 2,56–8,7 % (Lehrfeld, 1994). V semenech luštěnin se fytát vyskytuje převážně v proteinových orgánech endospermu nebo dělohy, ve kterých je obsaženo více než 90 % celkového přítomného fytátu. V semenech olejnin se obsah fytové kyseliny pohybuje od 1 do 5,4 % (tab. 2, Wise, 1983). U speciálních potravinářských produktů, jako jsou loupaná sezamová semena, proteinový koncentrát semen řepky olejné nebo sojový koncentrát, byl nalezen fytát v koncentraci až 10,7 %. Vysoká koncentrace fytátů byla nalezena v různých druzích ořechů. Obsahy fytátu ve vybraných potravinách shrnuje tab. 2 (Schlemmer, 2009 a reference citované v tomto článku). Uvedená velká rozpětí koncentrací kyseliny fytové nebo fytátu odrážejí nejen rozdíly botanických odrůd semen, vliv různého životního prostředí a klimatických podmínek pěstování, ale také různá stadia zralosti osiva. Všechny tyto faktory spolu s rozdíly vyplývajícími z použití různých analytických metod ovlivňují stanovený obsah kyseliny fytové.
 Tab. 1 Obsah fytové kyseliny v obilovinách
Tab. 1 Obsah fytové kyseliny v obilovinách
 Tab. 2 Obsah fytové kyseliny v dalších vybraných plodinách a potravinách
Tab. 2 Obsah fytové kyseliny v dalších vybraných plodinách a potravinách
3 VÝZNAM FYTOVÉ KYSELINY
Fytová kyselina tvoří pevné vazby s řadou důležitých minerálních prvků – hořčíku, draslíku, zinku, vápníku, fosforu a mědi a vytváří tak komplexní, pro organismus velmi obtížně stravitelné směsi. Proto byla dříve považována za antinutriční látku, která negativně ovlivňuje využití těchto prvků u zvířat i lidí. To může být stále problémem v oblastech, kde je vysoký alimentární příjem obilnin a luštěnin spojen s nedostatečným příjmem stopových minerálů, zejména železa a zinku.
Fytová kyselina je jednoznačně antinutriční látkou pouze u některých zvířat. Fytin dokážou beze zbytku strávit pouze přežvýkavci díky mikroorganismům v bachoru. Ostatní živočichové, včetně lidí, dokážou strávit fytin pouze částečně. Fytová kyselina je důvodem nízké využitelnosti fosforu obsaženého v obilí, luštěninách a olejninách u prasat a drůbeže. V místech s velkým rozšířením chovů zvířat je špatná stravitelnost fytové kyseliny hlavní příčinou znečištění povrchových vod fosfáty. Problém nízkého využití fytátového fosforu zvířaty je v současné době řešen přídavkem mikrobiální fytasy do krmné směsi (Marounek, 2004) nebo šlechtěním nových odrůd plodin se sníženým obsahem fytové kyseliny a zvýšenou hladinou fosforu nebo s vysokou přirozenou fytasovou aktivitou (Vaculová et al., 2012).
Ve výživě lidí přijímajících vyváženou smíšenou stravu je však přítomnost fytové kyseliny v potravě prospěšná. Hraje významnou roli v prevenci řady civilizačních onemocnění. Je silným antioxidantem, potlačuje tvorbu reaktivních hydroxylových radikálů katalyzovanou železem a rovněž snižuje tvorbu cholesterolu (Graf a Eaton, 1990). Má příznivý vliv na lipidový metabolismus, brání vzniku ledvinových kamenů, používá se jako dietetický doplněk a komplexotvorné činidlo pro odstranění stop iontů těžkých kovů (Marounek, 2004). Fytovou kyselinu v menším množství doprovázejí parciální fosforečné estery myoinositolu. Teoreticky existuje 63 (= 26–1) necyklických a 3 cyklické estery (Velíšek a Hajšlová, 2009). Myoinositol-1,4,5-trisdihydrogenfosfát a myoinositol-1,3,4,5-tetrakisdihydrogenfosfát se např. uplatňují v regulaci intracelulárního obsahu vápníku, myoinositol-1,3,4,5,6-pentakisdihydrogenfosfát moduluje afinitu ke kyslíku, myoinositol-1,2,6-trisdihydrogenfosfát inhibuje srážení krevních destiček a má protizánětlivé účinky (Velíšek a Hajšlová, 2009). Nejvýznamnější jsou prokázané protinádorové účinky fytové kyseliny (Shamsuddin, 2002; Vucenik a Shamsuddin, 2006; Jenab a Thompson, 2002; Singh a Agarwal, 2005).
Fytová kyselina má význam i v potravinářství, používá se jako aditivní látka pro čiření vín (zajišťuje odstranění železitých iontů vysrážením fytátu železitého) nebo k prevenci enzymatického i neenzymatického hnědnutí jablečného džusu inhibicí polyfenoloxidasy během výroby a skladování (Du et al., 2012).
4 FYTASY
Fosfor a další látky vázané ve fytinu mohou být rostlinami i živočichy využity až poté, co je fytin rozložen působením enzymů zvaných souhrnně fytasy. Fytasy postupně katalyzují hydrolýzu fytové kyseliny na meziprodukty myoinositolu (IP6, IP5, IP4, IP3, IP2, IP) a myoinositol. Enzymy schopné hydrolýzy fytátů se vyskytují v mikroorganismech, rostlinách a živočiších (Bitar a Reinhold, 1972; Irving a Cosgrove, 1971; Powar a Jagannathan 1967; Nayani a Markakis, 1984). Fytasy se řadí k fosfatasam a dělí se podle toho, kterou fosfátovou skupinu ve fytové kyselině nejprve odštěpí, na 3-fytasy (EC 3.1.3.8) a 6-fytasy (EC 3.1.3.26). 3-Fytasy jsou především mikrobiálního, zatímco 6-fytasy hlavně rostlinného původu. Rostlinné fytasy se vyskytují zejména v obilných zrnech, jejich aktivita je závislá na druhu obilniny. Nejvyšší aktivita fytas byla zjištěna v žitě, nižší potom v pšenici, ovsu a kukuřici (Greiner a Egli, 2003). Fytasy začnou rozkládat fytin, až když nastanou optimální podmínky. Nejdůležitějším požadavkem je vlhkost. Takové podmínky jsou splněny například při klíčení semen. Během výroby sladu se obsah fytátu oproti ječmenu sníží přibližně o 26 % (Hégrová, 2006). Při zpracování potravin, zejména při namáčení, klíčení, sladování, kvašení a výrobě pečiva, jsou přídavky rostlinné nebo mikrobiální fytasy široce používány ke snížení obsahu fytátu v potravinách s cílem zlepšit biologickou dostupnost minerálů a stopových prvků.
5 STANOVENÍ FYTOVÉ KYSELINY
5.1 Nespecifické metody
Stanovení obsahu fytové kyseliny zahrnuje její extrakci ze vzorku, většinou pomocí kyseliny chlorovodíkové nebo trichloroctové, eventuální přečištění pomocí ionexů a následující analytické stanovení. Základním předpokladem je to, aby byla extrahována či čištěna pouze fytová kyselina, neboť při zpracování potravin dochází k její hydrolýze a rozkladu.
První výzkumy byly nejčastěji založeny na vytvoření sraženiny s trojmocným železem. První obecně přijatá metoda na stanovení kyseliny fytové byla navržena v roce 1914 (Heubner a Stadtler, 1914) a byla založena na titraci v přítomnosti thiokyanátu amonného. Bod ekvivalence však nebyl ostrý z důvodu přítomnosti koloidní sraženiny fytátu železitého, která se během titrace tvoří. Casares a Moreno (1951) později tuto metodu modifikovali nahrazením indikátoru salicylátem sodným. Young (1936) vyvinul kolorimetrickou metodu ke stanovení fytové kyseliny založenou na odstranění sraženiny fytátu železitého centrifugací, vhodnou i pro nízká množství fytové kyseliny. Haug a Lantzsch (1983) tuto metodu později urychlili zahříváním vzorku přímo s roztokem trojmocného železa a sledováním poklesu obsahu železa kolorimetricky přidáním thioglykolové (merkaptooctové) kyseliny s 2,2‘ bipyridinem. Další metody stanovení byly založeny na komplexometrické titraci (Garcia-Villanova et al., 1982). Jednalo se o nepřímé stanovení založené na stechiometrickém poměru železitého iontu a fytátu (Common, 1940; Samotus a Schwimmer, 1962). Harland a Oberleas (1977) zjednodušili srážecí krok a extrahovali kyselinu fytovou přímo s 1,2 % HCl, následovala iontově výměnná chromatografie k oddělení anorganického fosforu s následným vyluhováním koncentrovanou H2SO4 a HNO3. Stanovený fosfor v potravinách převedli na ekvivalent fytátu. Tato metoda ovšem nerozlišuje mezi různými organickými fosfáty, které mohou být kromě fytátu přítomné ve vzorku (další inositolfosfáty nebo nukleotidy). Proto může být stanovený obsah kyseliny fytové chybně nadhodnocen. Protože však tato metoda byla aplikována především na surové a nezpracované potraviny s nízkým obsahem (do 15 %) nižších fosforylovaných inositolfosfátů (IP1 – IP5) (Dorsch et al., 2003), byla tato chyba prakticky nevýznamná. Uvedený postup se stal základem pro vývoj AOAC (Association of Analytical Communities) metody č. 986.11 pro určení obsahu fytátu v potravinách (AOAC, 1986). Další nespecifické metody jsou shrnuty v rozsáhlých review (Oberleas et al., 1986; Xu et al., 1992).
V roce 1980 Latta a Eskin vyvinuli rychlou a jednoduchou kolorimetrickou metodu na stanovení fytátu, založenou na reakci železitého iontu a sulfosalicylové kyseliny (Wadeovo činidlo). Výše uvedené metody jsou však nejvhodnější pro nezpracované potraviny s vysokým obsahem fytové kyseliny ve formě IP6, neboť jej nelze oddělit od nižších substituovaných inositolfosfátů. Tyto metody jsou také časově náročné, vyžadují pečlivé sledování, aby se minimalizovaly ztráty, a nelze jimi oddělit další interferující látky, které mohou komplikovat stanovení.
Pro stanovení ve zpracovaných potravinách s vysokým obsahem produktů hydrolýzy fytátu (nižších inositolfosfátů) nebo pro stanovení v biologických vzorcích (krevní plasma, moč, tkáně a pletiva) jsou tyto metody nedostatečné a nepřesné. Pro oddělení fytové kyseliny od nižších inositolfosfátů a dalších látek přítomných zejména v komplexních matricích bylo nutné vyvinout modernější, citlivější metody, které umožňují stanovení těchto látek i ve stopových koncentracích.
5.2 Chromatografické metody
Metody vysokoúčinné kapalinové chromatografie (HPLC) mají citlivost a reprodukovatelnost potřebnou k měření nízkých koncentrací v různých produktech, takže jsou vhodné pro kvantifikaci fytové kyseliny i ve zpracovaných potravinách. Mohou současně oddělit a určit IP6 a nižší fosforylované deriváty za současného zkrácení extrakce a zakoncentrování. S různými modifikacemi pro kolony, mobilní fáze, průtoky, extrakční rozpouštědla a techniky přípravy se HPLC stala standardní metodou pro rutinní analýzy kyseliny fytové. Nevýhodou je, že tyto metody jsou drahé a vyžadují značné investice do vybavení laboratoře.
V roce 1952 Smith a Clark jako první rozdělili fytovou kyselinu a další inositolfosfáty z půdy pomocí iontově-výměnné chromatografie. Jako mobilní fáze byl použit gradient HCl. V roce 1980 stanovil Tangendjaja et al. obsah fytové kyseliny v rýži kapalinovou chromatografií na reverzní fázi na koloně μBondapak C18 s pomocí 5 mM octanu sodného jako mobilní fáze. Graf a Dintzis (1982) postup zdokonalili, před touto separací přidali přečištění vzorku pomocí iontově výměnné chromatografie a pro detekci fytové kyseliny použili detektor indexu lomu (RI detekci). Uvedený postup úpravy a zakoncentrování vzorku se ukázal být velmi užitečným pro dobrou separaci a detekci inositolfosfátů metodami HPLC, zejména v komplexní matrici, a byl velmi často používán. Vzhledem k nízké retenci fytové kyseliny (1,4 min) na koloně μBondapak C18 mohly být další inositol fosfáty diskriminovány. Sandberg a Ahderinne (1986) rozdělili inositolfosfáty s různými počty fosfátových skupin (IP3-IP6) na stacionární fázi C18 s použitím octové kyseliny, methanolu a tetrabutylamoniumhydroxidu jako ion-párového činidla v mobilní fázi. Většina inositolfosfátů včetně jejich stereoisomerů byla rozdělena na silné anexové koloně MonoQ-column s použitím gradientu HCl (Mayr, 1988). Nevýhodou byl poměrně dlouhý čas analýzy (60–90 minut). Dobrého rozdělení inositol fosfátů (IP3-IP6) bylo dosaženo také na krátké koloně Mono-Q HR 5/5 (5×50 mm) za méně než 30 minut (Schlemmer et al., 2001). Tato metoda je dostačující pro většinu analýz fytové kyseliny v potravinářských a biologických vzorcích.
Použití spektrofotometrické detekce je vždy problematické, neboť fytová kyselina nemá charakteristické absorpční spektrum v ultrafialové a viditelné oblasti (UV-VIS). Proto se provádí nepřímá detekce, založená na stechiometrické reakci výměny kovu z barevného komplexu. Vysoká afinita fosfátových skupin inositol fosfátů k polyvalentním kationtům, jako např. Fe³⁺, Y³⁺ a Cu²⁺, je základem nejčastěji používaných metod pro UV- VIS detekci fytátu a inositolfosfátu. Absorpce může být měřena buď přímou interakcí mezi kationty, například Fe³⁺ ionty a inositol fosfáty (Phillippy, 2003), nebo prostřednictvím reakcí výměny ligandu, např. odstraněním kationtu z intenzivně barevného komplexu s inositolfosfáty, což vede k zesvětlení tohoto komplexu (Mayr, 1988). Metody poskytují spolehlivou detekci inositolfosfátů, nicméně tímto způsobem lze stanovit také jiné organické fosfáty, například nukleotidy, které během chromatografické separace mohou koeluovat s některými izomery nižších inositol fosfátů (IP1-IP3) a komplikovat tak stanovení. V případě analýzy potravinářských vzorků je tento vliv nízký, ale v případě analýzy buněk, tkání, krevní plasmy a dalších biologických vzorků musí být přítomné nukleotidy a další fosforylované proteiny odděleny již při přípravě vzorků, např. přidanou iontově-výměnnou chromatografií nebo úpravou pomocí aktivního uhlí. V roce 2006 Dost a Tokul navrhli HPLC metodu založenou na reakci výměny kovu z barevného komplexu Fe(III) thiokyanátu. Mayr (1988) použil k detekci inositol fosfátů barevného komplexu Ytria a 4-(2-Pyridylazo)resorcinolu (PAR). Ytrium-PAR komplex v přítomnosti inositol fosfátů zesvětlá, vzhledem k vyšší afinitě Y³⁺ iontů na jejich fosfátové skupiny. Absorbance je měřena při 546 nm jako negativní pík. Jde o dosud nejcitlivější detekci isomerů inositol fosfátů (pmol). Lze také použít postkolonové derivatizace (Phillippy a Johnston, 1985; Imanari et al., 1982; Cilliers a Niekerk, 1986).
Reakce na principu výměny ligandu byla uplatněna i u fluorescenční detekce inositolfosfátů, kde Irth (1990) odstranil Fe³⁺ ionty z komplexu Fe³⁺ a 4-methylkumarin-6-methyliminodioctové kyseliny s inositolfosfáty, čímž dojde k oslabení zhášení fluorescence v přítomnosti Fe³⁺ iontů a v závislosti na koncentraci inositolfosfátů se intenzita fluorescence zvýší. March (1999) použil metodu, založenou na aktivaci oxidace 2,2‘-bipyridyl ketonu hydrazonu katalyzovanou Cu2+ ionty vedoucí ke vzniku vysoce fluoreskujících produktů, ke stanovení fytátů v moči.
K detekci fytové kyseliny po HPLC separaci byla použita také detekce rozptylu světla (Phillippy et al., 2003), která byla méně citlivá, a vodivostní detekce, která je schopná s vysokou citlivostí detekovat i nižší inositolfosfáty (Talamond et al., 2000).
HPLC s hmotnostně spektrometrickou detekcí (LC/MS) byla rovněž použita pro stanovení fytátů v lidské moči (Perello et al., 2004). Metoda je založena na hydrolýze fytátu a stanovení myoinositolu po přečištění na anexové chromatografii. K separaci byla použita kolona Aminex HPX-87C, mobilní fází byla deionizovaná voda. Postkolonově byl přidán 5 mM octan amonný. Byly detekovány kladné ionty m/z = 198, odpovídající aduktu myoinositolu a amonného kationtu.
5.3 Další specifické metody
Metoda kapilární izotachoforézy je přímá, rychlá a poměrně jednoduchá a je často využívána v praxi pro různé matrice (Blatný et al., 1995; Dušková et al., 2000; Vaculová et al., 2012). Analýza fytové kyseliny byla rovněž provedena pomocí atomové emisní spektrometrie s indukčně vázaným plasmatem (Grases et al., 2004). Stanovení fytátů v biologických vzorcích pomocí plynové chromatografie s hmotnostně spektrometrickou detekcí (March, 2001) je založeno na čištění anexovou chromatografií, hydrolýze fytátu na myoinositol a následné derivatizaci na trimethylsilyl derivát. Metoda má srovnatelnou citlivost s LC/MS, je však zdlouhavá a vyžaduje použití vysoce aktivních fytas s dostatečnou stabilitou.
Spektroskopie nukleární magnetické rezonance (NMR) je vynikající analytickou technikou vhodnou pro stanovení IP6 fosfátů a produktů jeho hydrolýzy (IP1-IP5) fosfátů včetně jejich různých stereoizomerů. Je to neinvazivní metoda, nabízí výhody vysoké přesnosti a specifičnosti, nevyžaduje složitou přípravu vzorků, umožňuje přímou detekci všech fosfátových sloučenin v jednom experimentu. 31P-NMR spektroskopie s vysokým rozlišením slouží k určení obsahu fytátu v rostlinách a v biologických vzorcích, k detekci jeho formy a vazby na ostatní komponenty, nebo ke studiu metabolismu a degradaci fytátu při zpracování potravin. NMR byla úspěšně aplikována v rutinní analýze k rozlišení anorganického fosfátu od různých inositolfosfátů v rostlinných extraktech a potravinových vzorcích (Cosgrove, 1980) a pro studium sloučenin obsahujících fosfor v intaktních tkáních a buněčných suspenzích. NMR vykazuje dobrou shodu ve srovnání s jinými analytickými metodami pro stanovení fytátu v potravinách (Mazzola et al. 1986; Kemme et al., 1999). Pro analýzu NMR není zapotřebí použití standardů inositolfosfátů. Metoda je také schopná rozlišit izomery, které nejsou rozděleny chromatografickou separací. Nízká citlivost metod NMR může způsobit určité potíže při zjišťování nízké koncentrace inositolfosfátů v biologických a fyziologických vzorcích, jako jsou buňky nebo tkáně, další nevýhodou je, že NMR analýzy jsou drahé a vyžadují kvalifikované odborné znalosti potřebné ke správné interpretaci komplexních spekter ze složitých biologických systémů včetně potravin.
Komerčně dostupný set firmy Megazyme stanovuje množství fytové kyseliny v zrnech jako množství celkového fosforu uvolněného z materiálu pomocí enzymu fytasy. U nezpracovaných materiálů se předpokládá, že veškerý měřený fosfor byl uvolněn z (IP6) a toto množství volného fosforu je následně přepočítáno na množství kyseliny fytové. Zpracované výrobky obsahují i nižší inositolfosfáty, ze kterých je uvolněn fosfor působením alkalické fosfatasy. Celkový fosfor je stanoven modifikovanou kolorimetrickou metodou (Phytic acid/phytate assay, Megazyme).
Costa-Bauza et al. (2012) vyvinuli jednoduchou kolorimetrickou metodu pro stanovení fytátu v moči. Vzorky jsou zakoncentrovány pomocí SPE a měřeny kolorimetricky s použitím Fe(III)-thiokyanátu. Fotometrické metody umožňující stanovení fytátu bez hydrolýzy molekuly byly úspěšně použity k měření obsahu fytátu v obilovinách, kořenech a biologických vzorcích, nicméně, s výjimkou stanovení využívajících YCl₃-PAR, nejsou dostatečně citlivé ke stanovení fytátu v biologických vzorcích bez předchozího zakoncentrování.
Pro jednoduchou, rychlou a přesnou detekci kyseliny fytové a fytasy byly vyvinuty nové biosenzory (Mak et al., 2004). Biosenzor pro detekci fytasy je založen na imobilizaci pyruvát oxidasy a detekci fosfátových iontů vyrobených hydrolýzou fytové kyseliny. Dvouenzymový biosenzor pro detekci kyseliny fytové je založen na postupné imobilizaci fytasy a pyruvátoxidasy a amperometrické detekci enzymaticky uvolňovaného peroxidu vodíku.
6 ZÁVĚR
Můžeme shrnout, že surové nezpracované potraviny obvykle obsahují kolem 90 % fytové kyseliny (IP6), zatímco ve zpracovaných výrobcích bývají různě vysoké podíly částečně defosforylovaných izomerů (IP1-IP5) vzniklých vlivem degradace fytasami nebo zpracovacích podmínek. Nespecifické a kolorimetrické metody jsou proto vhodné pro stanovení obsahu fytové kyseliny u surovin a nezpracovaných produktů, zatímco pro potravinové výrobky a další biologické matrice, které obsahují i nižší inositolfosfáty, je vhodnější použití moderních citlivých metod, například kapalinové chromatografie.
Výzkum fytové kyseliny nepochybně bude i v budoucnu patřit ke světově významným tématům a podle všeho bude zaměřen na získání dalších informací o dietárním příjmu fytové kyseliny, lepší pochopení její absorpce v zažívacím traktu, buněčný příjem inositolfosfátů, roli fytátu v metabolismu a jeho vlivu na lidské zdraví a v neposlední řadě na vývoj a aplikaci specifických analytických metod stanovení v potravinách a biologických vzorcích.